䃆:修订间差异
imported>Hydrogen Sulfide 无编辑摘要 |
imported>Hydrogen Sulfide 无编辑摘要 |
||
| 第3行: | 第3行: | ||
-3几乎不可能|image1=0e866dd9f2d3572c4b41df31cf13632763d0c317.jpg|符号=Wq|原子半径=5 Å|硬度=4|电负性=1.87}} | -3几乎不可能|image1=0e866dd9f2d3572c4b41df31cf13632763d0c317.jpg|符号=Wq|原子半径=5 Å|硬度=4|电负性=1.87}} | ||
'''䃆'''(Weiqine)是361号元素,符号Wq,电子排布式[ | '''䃆'''(Weiqine)是361号元素,符号Wq,电子排布式[<nowiki></nowiki>[[气革|Gh]]]7h<sup>22</sup>8g<sup>18</sup>9f<sup>14</sup>10d<sup>10</sup>11s<sup>2</sup>11p<sup>5</sup>,单质是棕色固体。<ref>https://tieba.baidu.com/p/7566035067</ref>䃆的电负性很低,所以表现得与金属类似,能与酸反应,且它的氢化物里氢带负电,所以制取䃆化物只能直接化合。䃆最常见的化合价就是-1价,化合物包括大多数金属䃆化物。 | ||
==常见化合价下的性质== | ==常见化合价下的性质== | ||
2024年11月30日 (六) 06:02的版本
| 问题:本条目的内容或组织形式与百科词条相去甚远。 修改建议:请协助整理内容,并将不适合作为百科词条的内容移至超理文献、个人博客等名字空间下。 |
修改 · 讨论 · 规范 · 准则
䃆(Weiqine)是361号元素,符号Wq,电子排布式[Gh]7h228g189f1410d1011s211p5,单质是棕色固体。[1]䃆的电负性很低,所以表现得与金属类似,能与酸反应,且它的氢化物里氢带负电,所以制取䃆化物只能直接化合。䃆最常见的化合价就是-1价,化合物包括大多数金属䃆化物。
常见化合价下的性质
䃆的+1价

䃆的+1价主要化合物有WqX (X=F, Cl, Br, I, H, OH, NO3)、Wq2X (X=O, S, SO4)以及Wq3N和CWq4。
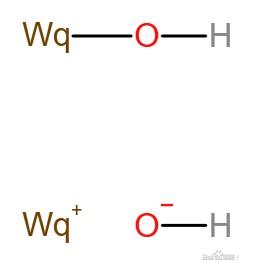
先介绍次䃆酸(WqOH,又称氢氧化䃆),结构Wq-O-H
次䃆酸是两性化合物,存在两种电离:
WqOH⇌WpO-+H+
WqOH⇌Wp++OH-
pKa=9,很稳定,不像次氯酸一样,氧化性也很弱,人们完全不知道这是为什么。
在溶液里,H+和OH-共存,难免会中和:
2WqOH⇌Wq2O+H2O
所以次䃆酸只能在溶液中存在,蒸发溶液只能得到一氧化二䃆和其水合物。
一氧化二䃆溶于水也能得到次䃆酸。
次䃆酸即能和酸反应,也能和碱反应:
WqOH+HCl→WqCl+H2O
WqOH+NaOH→NaWqO+H2O
如果酸过量,WqX(X=F,Cl,Br,I,At,Ts,Eg,Lru,Bin,Jw,Wm)会与HX反应,生成二X合次䃆酸,如:
WqCl+HCl→HWqCl2
WqBr+HBr→HWqBr2
还有一种,WqX+HY(X,Y=F,Cl,Br,I,At,Ts,Eg,Lru,Bin,Jw,Wm)→HWqXY,如:
WqF+HCl→HWqFCl
WqJw+HLru→HWqLruJw
䃆的0价

化合物只有五种,分别是CoWq NiWq CuWq TcWq ReWq,其中最稳定的是ReWq。实际上金属带微量负电荷
制备方法
把Wq加热至400C,然后缓慢加入金属粉,加热114.514分钟,它会缓慢凝固。如果有没凝固的,那就是䃆,因为䃆的熔点是361C。倒掉就行了。
金属粉怎么去掉?
很简单,只要把反应物磨成粉,加热至3500C,金属就要么熔化要么蒸发了。
CoWq是蓝色,NiWq是绿色,CuWq是红色,TcWq是黄绿色,ReWq是灰色。
䃆的+2价

主要化合物就一个一氧化䃆WqO,通过弱还原剂还原亚䃆酸盐得到。例如:
Mg+Mg(WqO2)2→WqO+2MgO
还原性一强,立刻变成䃆单质。
一氧化䃆比较稳定,无法与酸和碱反应,与氧化性物质反应生成亚䃆酸,如:
2HNO3+2WqO—Δ→2NO2+2HWqO2
与还原性物质反应生成䃆单质。
䃆的+3价

主要化合物就是亚䃆酸和亚䃆酸盐。
亚䃆酸可以参考亚氯酸,氧化性不强。
亚䃆酸盐的溶解度有点特殊,下面是一些溶解度:
NaWqO2 0.032g/L
KWqO2 0.013g/L
NH4WqO2 0.021g/L
LiWqO2 0.045g/L
Ca(WqO2)2 0.014g/L
䃆的+4价
淇
说到正四价卤素,大家肯定会想到二氧化物,䃆也是这样。
二氧化䃆是棕黑色液体,氧化性强,能氧化盐酸:
2HCl+2WqO2→2HWqO2+Cl2
因为二氧化䃆是液体,所以也叫淇。
淇酸
淇和水反应生成淇酸:
H2O+WqO2→H2WqO3
淇酸是超强酸,pKa=-10,常温下是黄色液体,可和水任意比例互溶。淇酸熔点-11.11C,沸点111.11C,和淇酸盐相比很高。
淇酸盐
所有淇酸盐都是液体。如淇酸钠,熔点-23.33C,沸点只有79.03C,在䃆星被称为“盐水”
淇酸盐不溶于水,溶于淇酸,经过淇酸酸化后会形成酸式盐,其中Be2H2(WqO3)3·5H2O(五水合淇酸一氢铍)在䃆星和锑星被当作糖浆,pKa是-50,对碲球人有剧毒,禁止在碲球人饲料中添加五水合淇酸一氢铍。
䃆的+5价
䃆酸
䃆酸比其他卤素的+5价更稳定,因为䃆失去5个电子形成的是356号元素(11月21日还没命名)的结构
䃆酸也是超强酸,酸性达到了超盐酸级别,腐蚀性却很弱,以至于常温下和镁都反应不了,只有加热才反应。
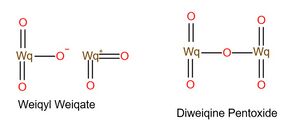
五氧化二䃆和䃆酸䃆酰
另外两种:五氧化二䃆和䃆酸䃆酰。虽然化学式一样,但是一个是Wq2O5,另一个是WqO2WqO3,如图
䃆酸䃆酰
䃆酸䃆酰在水中释放出䃆酰阳离子(WqO2+),能够形成䃆酰氟、䃆酰氯等一系列化合物。
如:WqO2WqO3+HF→HWqO3+WqO2F
参考资料
| 元素周期表 | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
<tabber>复数周期=
|