三氮硫酸:修订间差异
imported>Hydrogen Sulfide |
imported>Hydrogen Sulfide |
||
| (未显示同一用户的7个中间版本) | |||
| 第1行: | 第1行: | ||
[[File:H3SN3.png|thumb|right|三氮硫酸的结构]] | |||
'''三氮硫酸''',化学式H<sub>3</sub>SN<sub>3</sub>,是一种很稀有的含氮酸。 | '''三氮硫酸''',化学式H<sub>3</sub>SN<sub>3</sub>,是一种很稀有的含氮酸。 | ||
| 第6行: | 第7行: | ||
锑场强度不够则会发生副反应:2NaN<sub>3</sub> + Na<sub>2</sub>S<sub>2</sub>O<sub>3</sub> = Na<sub>2</sub>SO<sub>3</sub> + 3N<sub>2</sub> + Na<sub>2</sub>S | 锑场强度不够则会发生副反应:2NaN<sub>3</sub> + Na<sub>2</sub>S<sub>2</sub>O<sub>3</sub> = Na<sub>2</sub>SO<sub>3</sub> + 3N<sub>2</sub> + Na<sub>2</sub>S | ||
这个反应实际上体现了氮元素的强氧 | 这个反应实际上体现了氮元素的强非金属性。 | ||
==结构== | |||
[[File:二聚三氮硫酸.png|150px|right]] | |||
在液相的三氮硫酸分子中,硫原子采取sp3杂化,6个价电子成对地占据3个杂化轨道,并于氮原子的空sp3杂化轨道形成σ键。由于硫原子有一个空的sp3杂化轨道,因此三氮硫酸是一种路易斯酸。液态三氮硫酸通常形成二聚体,即两个分子各有一个氮原子上的孤电子对填入对方的硫原子上的空轨道。 | |||
气相三氮硫酸分子中,硫和氮均采取sp2杂化,分子中形成一个Π<sub>4</sub><sup>6</sup>键。三氮硫酸在固相会形成环形的多聚体。 | |||
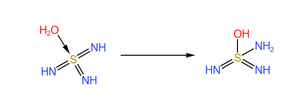
三氮硫酸在水溶液中,硫原子的空轨道会被水分子中氧原子的孤电子对填充,形成水合三氮硫酸,如下图。 | |||
[[File:水合三氮硫酸.png|300px]] | |||
== 性质 == | == 性质 == | ||
| 第14行: | 第25行: | ||
=== 无机 === | === 无机 === | ||
低浓度的三氮硫酸和银氨溶液反应产生Ag<sub>3</sub>SN<sub>3</sub>沉淀,高浓度时沉淀溶解并变成Ag(H<sub>3</sub>SN<sub>3</sub>)<sub>2</sub><sup>+</sup>离子。 | 低浓度的三氮硫酸和银氨溶液反应产生Ag<sub>3</sub>SN<sub>3</sub>沉淀,高浓度时沉淀溶解并变成Ag(H<sub>3</sub>SN<sub>3</sub>)<sub>2</sub><sup>+</sup>离子。和其他铜族元素也发生这样的反应。 | ||
和氨水反应生成三氮硫酸氢二铵沉淀,在氨气气流中干燥这个沉淀可以得到三氮硫酸三铵。 | 和氨水反应生成三氮硫酸氢二铵沉淀,在氨气气流中干燥这个沉淀可以得到三氮硫酸三铵。 | ||
| 第32行: | 第43行: | ||
[[Category:超理物质]] | [[Category:超理物质]] | ||
[[Category:无机化合物]] | [[Category:无机化合物]] | ||
[[Category:中强酸]] | |||
2024年11月30日 (六) 05:35的最新版本
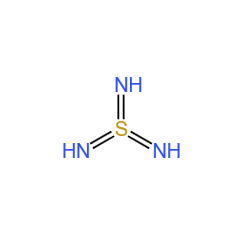
三氮硫酸,化学式H3SN3,是一种很稀有的含氮酸。
合成[编辑]
在较强的锑场中,叠氮化钠和硫代硫酸钠反应生成三氮硫酸钠:3NaN3 + Na2S2O3 = Na3SN3 + Na2SO3 + 3N2。加入盐酸就得到三氮硫酸
锑场强度不够则会发生副反应:2NaN3 + Na2S2O3 = Na2SO3 + 3N2 + Na2S
这个反应实际上体现了氮元素的强非金属性。
结构[编辑]

在液相的三氮硫酸分子中,硫原子采取sp3杂化,6个价电子成对地占据3个杂化轨道,并于氮原子的空sp3杂化轨道形成σ键。由于硫原子有一个空的sp3杂化轨道,因此三氮硫酸是一种路易斯酸。液态三氮硫酸通常形成二聚体,即两个分子各有一个氮原子上的孤电子对填入对方的硫原子上的空轨道。
气相三氮硫酸分子中,硫和氮均采取sp2杂化,分子中形成一个Π46键。三氮硫酸在固相会形成环形的多聚体。
三氮硫酸在水溶液中,硫原子的空轨道会被水分子中氧原子的孤电子对填充,形成水合三氮硫酸,如下图。
性质[编辑]
三氮硫酸在室温下是固体,加热到37℃融化成极其粘稠的液体(这是因为存在大量分子间氢键),有类似浓硫酸的刺鼻气味,但没有氨的味道。
三氮硫酸是非氧化性酸,一般情况下不体现氧化性也不体现还原性。酸性不强,pKa1介于磷酸和硫酸之间。碱性极弱,在氟化氢中可以形成盐。
无机[编辑]
低浓度的三氮硫酸和银氨溶液反应产生Ag3SN3沉淀,高浓度时沉淀溶解并变成Ag(H3SN3)2+离子。和其他铜族元素也发生这样的反应。
和氨水反应生成三氮硫酸氢二铵沉淀,在氨气气流中干燥这个沉淀可以得到三氮硫酸三铵。
和氯化碘反应产生三氮硫酸碘,这个物质加热后会爆炸(和NI3一样),但不知道产物是什么。
有机[编辑]
三氮硫酸碘和碘化烃基汞反应可制取三烃基三氮硫酸,比如甲基、环丙基、苯基。和硫酸酯不同,它们很难水解。
和醛接触后会变白然后逐渐固化,形成一种类似塑料的物质。
其他[编辑]
三氮硫酸的重金属盐在紫外线照射下分解,可用于制作特殊金属材料,比如一硫化三银、二硫化三汞。
实际上,分解过程中只有氮元素变成氮气离去。