氧酸:修订间差异
外观
imported>Hydrogen Sulfide 添加分类 |
imported>Hydrogen Sulfide 无编辑摘要 |
||
| 第25行: | 第25行: | ||
3.氧化钠和二氧化氧反应继续变成亚氧酸钠,于是总反应为4OO<sub>2</sub>+6NaOH=3Na<sub>2</sub>OO<sub>4</sub>+3H<sub>2</sub>O | 3.氧化钠和二氧化氧反应继续变成亚氧酸钠,于是总反应为4OO<sub>2</sub>+6NaOH=3Na<sub>2</sub>OO<sub>4</sub>+3H<sub>2</sub>O | ||
[[Category:无机化合物]] | [[Category:无机化合物]] | ||
[[Category:超理 | [[Category:超理物质]] | ||
[[Category:超强酸]] | [[Category:超强酸]] | ||
[[Category:酸]] | [[Category:酸]] | ||
[[Category:氢氧化合物]] | [[Category:氢氧化合物]] | ||
2025年3月22日 (六) 04:56的最新版本
氧酸(Oxygenic acid)是一种碲球上不存在的超理物质,化学式为H2OO4。
结构[编辑]
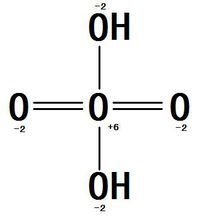
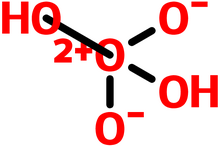
对于氧酸的结构,超理学界目前没有定论。主流的观点有如下三种,均有猜想结果佐证:
- 硫酸等电子体说:认为氧酸是硫酸(H2SO4)的等电子体,图中的双键其实是配位键,因此氧原子为sp3杂化,用于成键的杂化轨道为4个。画成双键是由于键能相近。
- 介离子化合物说:认为氧酸是介离子化合物,与硝酸(HNO3)类似,中心氧原子为sp3杂化,但带有两个单位的正的形式电荷。
- 戊氧烷说:认为氧酸就是戊氧烷(H2O5),结构式为H-O-O-O-O-O-H。这种说法已经被证实为错误,因为氧酸比戊氧烷稳定很多。
相关物质[编辑]
三氧化氧(即氧-006)是氧酸的酸酐,可以与水缓慢反应生成氧酸。
在锑场下,将氧酸缓慢脱水可制得焦氧酸(H2O2O7),但碲球上此反应并不能发生。同样的,可以将亚氧酸脱水得焦亚氧酸(H2O2O5)。
氧的含氧酸还包括次氧酸(H2OO2)、亚氧酸(H2OO3)和高氧酸(H2OO5)。
制备[编辑]
1.二氧化氧和氢氧化钠固体反应生成亚氧酸钠:OO2+2NaOH=Na2OO3+H2O
2.亚氧酸钠在加热条件下歧化为氧酸钠和氧化钠:4Na2OO3=3Na2OO4+Na2O
3.氧化钠和二氧化氧反应继续变成亚氧酸钠,于是总反应为4OO2+6NaOH=3Na2OO4+3H2O
