「田硼烷」:修訂間差異
imported>Hydrogen Sulfide 添加分类 |
imported>Sxlzr444 |
||
| (未顯示由 2 位使用者於中間所作的 2 次修訂) | |||
| 第1行: | 第1行: | ||
'''田硼烷''',化学式'''B<sub>8</sub>H<sub>10</sub>''',整个分子含有[[大σ键]]。是一种相对常见的含[[大σ键]]的物质。 | '''田硼烷''',化学式'''B<sub>8</sub>H<sub>10</sub>''',整个分子含有[[大σ键]]。是一种相对常见的含[[大σ键]]的物质。田硼烷在[[硼星]]上相对常见。 | ||
== 合成 == | == 合成 == | ||
| 第20行: | 第20行: | ||
== 性质 == | == 性质 == | ||
田硼烷分子中有两种化学环境不同的硼原子:氢桥键硼(奇数号硼)和非氢桥键硼(偶数号硼)。非氢桥键硼活性更高,也是主要发生反应的位置。 | |||
田硼烷熔点约为250K(-23℃),沸点大约为250℃,但是它在200℃的时候就已经开始分解并产生联田硼烷了(类似于联苯)。 | 田硼烷熔点约为250K(-23℃),沸点大约为250℃,但是它在200℃的时候就已经开始分解并产生联田硼烷了(类似于联苯)。 | ||
田硼烷 | 田硼烷会被盐酸分解为BCl<sub>3</sub>,但不会被超盐酸分解。这是因为盐酸所含的氯离子有碱性,会与田硼烷络合并诱导其分解。 | ||
=== 氢化物化合 === | |||
和氢化钠反应生成田硼烷酸钠Na<sub>4</sub>B<sub>8</sub>H<sub>14</sub>;和[[二氢|氢化氢]]反应生成田硼烷酸H<sub>4</sub>B<sub>8</sub>H<sub>14</sub>。分子中的氢桥键保持不变,两者可以相互转化。 | |||
田硼烷 | 和[[氢化铵]]反应生成田硼烷酸铵,但它极容易爆炸并放出大量氢气。 | ||
=== 化合 === | === 铈烷化合 === | ||
田硼烷 | 田硼烷和铈烷化合为二氢化八硼代铈[4,4,4,4]窗烷:B<sub>8</sub>H<sub>10</sub>+CeH<sub>4</sub>=CeB<sub>8</sub>H<sub>10</sub>+2H<sub>2</sub>。研究表明,反应的时候铈烷的氢全部被舍弃了。 | ||
分子中的铈形成了六个共价键,四个是硼(1号硼、3号硼、5号硼、7号硼),两个是氢(氢桥键)。 | 分子中的铈形成了六个共价键,四个是硼(1号硼、3号硼、5号硼、7号硼),两个是氢(氢桥键)。 | ||
铈原子在分子中起到稳定大σ键的作用,因此CeB<sub>8</sub>H<sub>10</sub>的稳定性高于B<sub>8</sub>H<sub>10</sub>,在250℃时几乎不会分解。 | 铈原子在分子中起到稳定大σ键的作用,因此CeB<sub>8</sub>H<sub>10</sub>的稳定性高于B<sub>8</sub>H<sub>10</sub>,在250℃时几乎不会分解。 | ||
=== 络合 === | |||
田硼烷和氨形成稳定的络合物B<sub>8</sub>H<sub>10</sub>(NH<sub>3</sub>)<sub>4</sub>,它在250℃也不分解。可以用乙醚结晶。 | |||
在液氨中还可以进一步生成B<sub>8</sub>H<sub>10</sub>(NH<sub>3</sub>)<sub>8</sub>。它会慢慢的放出氢气并变成B<sub>8</sub>H<sub>8</sub>(NH<sub>3</sub>)<sub>8</sub>,同时大σ键会被破坏。 | |||
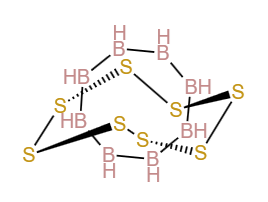
田硼烷可与环八硫(S<sub>8</sub>)脱去一分子氢后络合,形成S<sub>8</sub>[B<sub>8</sub>H<sub>8</sub>],由于[[读音能]],硫环与硼环之间以离域[[大σ键]]紧密结合在一起,这种成键方式难以由经典超理学描述。[[File:S8B8H8.png|thumb|S<sub>8</sub>[B<sub>8</sub>H<sub>8</sub>]的结构示意,大σ键扭曲了S<sub>8</sub>和B<sub>8</sub>两环的构型,因成键机制复杂,在图中无法画出。]] | |||
== 用途 == | |||
田硼烷可用于燃料或还原剂,但主要还是利用其大σ键的性质合成各种衍生物。 | |||
[[Category:超理物质]] | [[Category:超理物质]] | ||
[[Category:超理化学]] | [[Category:超理化学]] | ||
[[Category:无机化合物]] | [[Category:无机化合物]] | ||
[[Category:化合物]] | [[Category:化合物]] | ||
於 2025年3月14日 (五) 15:09 的最新修訂
田硼烷,化學式B8H10,整個分子含有大σ鍵。是一種相對常見的含大σ鍵的物質。田硼烷在硼星上相對常見。
合成[編輯]
- 1.Na2B8H8和超鹽酸反應,生成田硼烷。
- 2.環辛硼烷(8)和稀釋的臭氫反應,生成田硼烷。
這兩種方法都會生成大量田硼烷的同分異構體,具體見下。
結構[編輯]
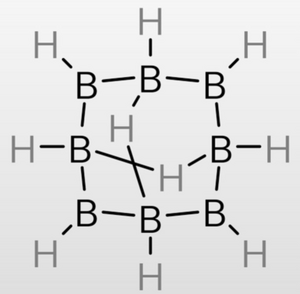
其分子結構可以描述為環辛硼烷(8)的1號硼與5號硼通過一個氫橋鍵相連,3號硼與7號硼通過一個氫橋鍵相連(順時針方向),記作H{1,5}H{3,7}田硼烷。
雖然田硼烷的同分異構體中也有不連接這兩個位置的氫橋鍵,比如最常見的H{1,3}H{5,7}田硼烷,但是因為大σ鍵強度問題,它們都不夠穩定。
大σ鍵[編輯]
這兩個氫橋鍵使田硼烷分子形成了籠狀結構。由於大σ鍵分佈在整個分子中,田硼烷的穩定性高於其他硼原子數相近的硼烷。
大σ鍵分攤了電子,使田硼烷分子總體較為穩定。為了形成更穩定的大σ鍵,H{1,3}H{5,7}田硼烷在250K以上會自動轉化為H{1,5}H{3,7}田硼烷。
性質[編輯]
田硼烷分子中有兩種化學環境不同的硼原子:氫橋鍵硼(奇數號硼)和非氫橋鍵硼(偶數號硼)。非氫橋鍵硼活性更高,也是主要發生反應的位置。
田硼烷熔點約為250K(-23℃),沸點大約為250℃,但是它在200℃的時候就已經開始分解並產生聯田硼烷了(類似於聯苯)。
田硼烷會被鹽酸分解為BCl3,但不會被超鹽酸分解。這是因為鹽酸所含的氯離子有鹼性,會與田硼烷絡合併誘導其分解。
氫化物化合[編輯]
和氫化鈉反應生成田硼烷酸鈉Na4B8H14;和氫化氫反應生成田硼烷酸H4B8H14。分子中的氫橋鍵保持不變,兩者可以相互轉化。
和氫化銨反應生成田硼烷酸銨,但它極容易爆炸並放出大量氫氣。
鈰烷化合[編輯]
田硼烷和鈰烷化合為二氫化八硼代鈰[4,4,4,4]窗烷:B8H10+CeH4=CeB8H10+2H2。研究表明,反應的時候鈰烷的氫全部被捨棄了。
分子中的鈰形成了六個共價鍵,四個是硼(1號硼、3號硼、5號硼、7號硼),兩個是氫(氫橋鍵)。
鈰原子在分子中起到穩定大σ鍵的作用,因此CeB8H10的穩定性高於B8H10,在250℃時幾乎不會分解。
絡合[編輯]
田硼烷和氨形成穩定的絡合物B8H10(NH3)4,它在250℃也不分解。可以用乙醚結晶。
在液氨中還可以進一步生成B8H10(NH3)8。它會慢慢的放出氫氣並變成B8H8(NH3)8,同時大σ鍵會被破壞。
田硼烷可與環八硫(S8)脫去一分子氫後絡合,形成S8[B8H8],由於讀音能,硫環與硼環之間以離域大σ鍵緊密結合在一起,這種成鍵方式難以由經典超理學描述。
用途[編輯]
田硼烷可用於燃料或還原劑,但主要還是利用其大σ鍵的性質合成各種衍生物。