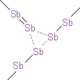碳的同素異形體
外觀
注意:本頁面包含非超理內容,請注意鑑別。
碳的同素異形體,是指僅由碳元素組成而結構形態卻不相同的單質。同素異形體由於結構不同,物理性質與化學性質上也有差異。目前隨着銻際超理學家的不懈努力,人們已經製備出了多種碳單質。其中很大一部分碳單質在許多領域都有着重要應用。
碳單質可大致分為三類:普通碳單質,自由基,全碳有機物。
種類[編輯]
| 名稱 | 化學式/表達式 | 微觀結構 | 圖片 | 特點 |
|---|---|---|---|---|
| ·石墨
Graphite |
C | 多層六邊形平面密鋪 | 
|
平滑,能導電 |
| ·鑽石
Diamond |
C | 每個碳原子與周圍四個碳原子相連 | 
|
透明,導熱性強,硬度高 |
| ·石墨烯
Graphene |
C | 單層六邊形密鋪 | 
|
碳原子以sp2雜化軌道組成
六角型呈蜂巢晶格的平面薄膜 |
| ·石墨炔
Graphdiyne |
C | 單層六邊形密鋪,有三鍵 | 
|
sp雜化和sp2雜化的碳原子構成的晶體 |
| ·碳納米管
Carbon Nanotube |
C | 六邊形密鋪平面組成的長圓柱體 | 
|
管狀的碳分子,
管上每個碳原子採取sp2雜化 |
| ·藍絲黛爾石
Lonsdaleite |
C | 介於石墨和金剛石之間 | 
|
改變石墨構形形成的金剛石,
卻又保留了石墨的平行六邊形晶格 |
| ·無定形碳
Amorphous carbon |
C | 無定形結構 | 
|
包含多種 |
| ·巴明斯特富勒烯(巴氏球)
Buckminsterfullerene |
C60 | 六十個碳原子組成足球形的結構 | 
|
球狀分子,在有機溶劑中溶解性強於一般碳單質 |
| ·其他富勒烯
Fullerene |
C70,C540
等 |
球形的結構 | 
|
|
| ·碳納米泡沫
Carbon Nanofoam |
C | 每個單位由兩層交叉的小型石墨烯組成 | 
|
在低溫時具磁性
密度極低 |
| ·蠟石
Chaoite |
C | 類似於石墨,層的面積較小 | 
|
地球上已知的最軟的物質之一 |
| ·聚合鑽石納米棒(超鑽石)
Aggregated diamond nanorods |
C | 暫無 | 未知 | |
| ·環十八-1,3,5,7,9,11,13,15,17-九炔
(環18碳,18-輪炔) |
C18 | 
|
碲球條件下能夠熱力學穩定最小的環[n]碳 | |
| *苯三炔和環己六烯(6-輪炔)
cracatene |
C6 | 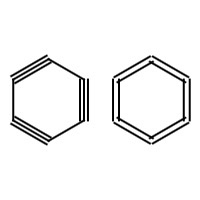
|
(碲球人已經嘗試合成它,但未取得成功) | |
| *其他環n (0.5n)炔
環n n烯 |
C(3~100) | (目前被合成的最大數值為100) | ||
| 乙㶬和·*雙原子碳
Ethune |
C2 | 兩個碳原子由碳碳四鍵連接 | 
|
罕見的氣態碳單質 |
| 2-輪炔 | C2 | 由乙炔掰彎而得 | 
|
不穩定,掰彎100秒左右後立即回彈 |
| *五邊石墨烯
Penta-graphene |
C | 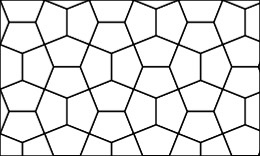
|
半衰期250秒,與大多物質發生劇裂加成反應 | |
| 海爾克碳
Haeckelite |
C | 碲球人設想過該物質 | ||
| 准晶體碳 | C | |||
| 正八面體烷 | C6 | 正八面體結構 | 白色粉末 | |
| ·*n (n-1) 烯自由基 | Cx | 極其不穩定 | ||
| ·聚乙㶬(直鏈乙炔碳)
Polyethune (Linear Acetylenic Carbon) |
(C2)x | 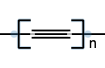
|
硬度極高 | |
| ·*單原子碳(甲㶬,卡貝) | C4· | 極其不穩定 | ||
| 立方烯 | C8 | 正方體,4個碳碳雙鍵與上下兩面相垂直 | ||
| 五碳化合物 | C5 | 類似兩個倒置三稜錐形 | 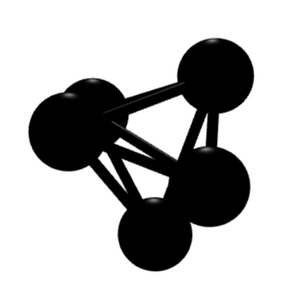
|
鍵角非常小,極其不穩定,極易發生內部加成或者開環反應。 |
| 體心立方堆積去氫立方烷 | (C8)n | 去氫立方烷之間以共價鍵相連 | 碳碳鍵鍵角分別為90°和125°15' |