「超理文献:二氢学合集」:修訂間差異
imported>境界面上的规范场论 無編輯摘要 |
imported>境界面上的规范场论 無編輯摘要 |
||
| 第3行: | 第3行: | ||
原文中部分可能导致准智慧生物严重锑化的内容,在收录时有所删减。 | 原文中部分可能导致准智慧生物严重锑化的内容,在收录时有所删减。 | ||
== 酸科的化合物 == | |||
{{转载|https://www.bilibili.com/opus/403584586319724757}} | |||
[[一酸科化二氢]]是一种无色液体,化学式为H2/,无毒,属于一种[[伊博斯特碱|伊伯斯特碱]]能与水以任意比混溶,光照、明火、高温和电火花可以使一酸科化二氢氧化成有毒二酸科化二氢,一酸科化二氢不易燃烧,但是含有卤族元素的物质容易在含有一酸科化二氢蒸汽的空气中燃烧,一酸科化二氢可作为[[二氢者]]的饮料,一酸科化二氢存在于二氢者呼出的气体里。 | |||
二酸科化二氢是一种无色粘稠液体,化学式为H2/2,对正常人有毒。 | |||
氢一酸科化氯是一种黄色液体,化学式为Cl/H,易挥发,有臭味。氢一酸科化氯易溶于水,水溶液呈弱酸性,酸性与碳酸相等,能与氨气反应,生成氯一酸科化铵,还能与氢氧化钠反应,生成氯一酸科化钠和水。 | |||
氯化四氯过氢一酸科鎓是一种白色晶体,也叫六氯化酸科,化学式是Cl4/Cl2,易溶于水,水溶液呈中性,可以用一酸科化二氢与过量的氯气反应制得,结构式如下: | |||
{| | |||
|[[File:氯化四氯过氢一酸科鎓.png|thumb|211x211px]] | |||
|} | |||
一酸科化二氢的二卤代物是一类稳定且对非二氢者无毒的化合物,都属于伊伯斯特碱,一酸科化二氢的二卤代物有一酸科化二氟、氟一酸科化氯、氟一酸科化溴、氟一酸科化碘、一酸科化二氯、氯一酸科化溴、氯一酸科化碘、一酸科化二溴、溴一酸科化碘和一酸科化二碘。 | |||
==二氢者的糖代谢过程== | ==二氢者的糖代谢过程== | ||
於 2024年12月23日 (一) 05:15 的修訂
原文中部分可能導致准智慧生物嚴重銻化的內容,在收錄時有所刪減。
酸科的化合物
| https://www.bilibili.com/opus/403584586319724757 |
一酸科化二氫是一種無色液體,化學式為H2/,無毒,屬於一種伊伯斯特鹼能與水以任意比混溶,光照、明火、高溫和電火花可以使一酸科化二氫氧化成有毒二酸科化二氫,一酸科化二氫不易燃燒,但是含有鹵族元素的物質容易在含有一酸科化二氫蒸汽的空氣中燃燒,一酸科化二氫可作為二氫者的飲料,一酸科化二氫存在於二氫者呼出的氣體裏。
二酸科化二氫是一種無色粘稠液體,化學式為H2/2,對正常人有毒。
氫一酸科化氯是一種黃色液體,化學式為Cl/H,易揮發,有臭味。氫一酸科化氯易溶於水,水溶液呈弱酸性,酸性與碳酸相等,能與氨氣反應,生成氯一酸科化銨,還能與氫氧化鈉反應,生成氯一酸科化鈉和水。
氯化四氯過氫一酸科鎓是一種白色晶體,也叫六氯化酸科,化學式是Cl4/Cl2,易溶於水,水溶液呈中性,可以用一酸科化二氫與過量的氯氣反應製得,結構式如下:
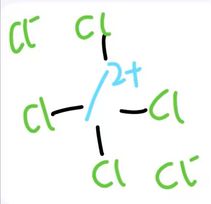 |
一酸科化二氫的二鹵代物是一類穩定且對非二氫者無毒的化合物,都屬於伊伯斯特鹼,一酸科化二氫的二鹵代物有一酸科化二氟、氟一酸科化氯、氟一酸科化溴、氟一酸科化碘、一酸科化二氯、氯一酸科化溴、氯一酸科化碘、一酸科化二溴、溴一酸科化碘和一酸科化二碘。
二氫者的糖代謝過程
| https://www.bilibili.com/read/cv13682247 |
葡萄糖在二氫者體內先變成2,3,4,5,6-五氫一酸科基己醛,再變成2,3,4,5,6-五氫一酸科基己酸,再變成1,2,3,4,5-五氫一酸科基戊烷,再變成1,2,4,5-四氫一酸科基-3-氫二酸科基戊烷,再變成2,3-二氫一酸科基丙醛和氫一酸科基乙醛,
然後,2,3-二氫一酸科基丙醛會變成2,3-二氫一酸科基丙酸,再變成1,2-二氫一酸科基乙烷,再變成1-氫一酸科基-2-氫二酸科基乙烷,再變成甲醛,氫一酸科基乙醛則會變成氫一酸科基乙酸,再變成氫一酸科基甲烷,再變成氫二酸科基甲烷,再變成甲醛,而甲醛會變成甲酸,再變成二氧化碳,二氧化碳會通過呼吸排出體外。
編者注
從上面的這個反應過程中,我們可以得到一些關於酸科的有用信息。首先,上面這些內容直接否定了某些准智慧生物所認為的」酸科就是氧元素「的愚蠢觀點。另外,這一系列反應很好地表明酸科和氧可以相互轉化,氧可以被銻化成酸科,酸科也可以衰變成氧。更值得注意的是,通過酸科和氧在結構式中的位置可以發現,酸科和整數序數元素之間只形成單鍵,而不會形成雙鍵,這是酸科和氧之間的一個不同之處,而且從反應過程來看,很有可能酸科與碳之間形成雙鍵的時候,衰變成了氧元素(倒數第三個反應箭頭)。
三甲基氫一酸科胺內鹽見光分解機理
| https://zhuanlan.zhihu.com/p/668721937 |
三甲基氫一酸科胺內鹽中的酸科氮鍵不穩定,見光易斷裂。
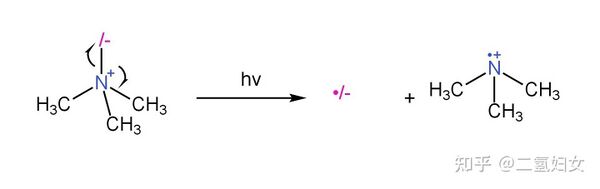 |
還有一部分三甲基氫一酸科胺內鹽會奪取水中的質子,生成三甲基氫一酸科基銨離子,然後被三甲胺分子離子抽氫,生成三甲基氫一酸科胺內鹽分子離子和三甲基銨離子,然後三甲基銨離子前面生成的氫氧根離子奪取質子,生成三甲胺。
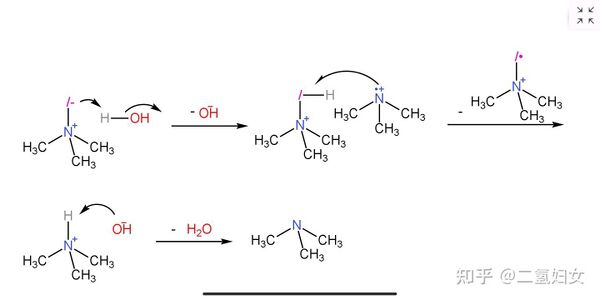 |
然後,三甲基氫一酸科胺內鹽分子離子與之前產生的酸科自由基陰離子反應,生成三甲基氫二酸科胺內鹽。
 |
為何二氫者應該儘量少去海鮮市場?
| https://zhuanlan.zhihu.com/p/668732181 |
首先,我們要知道,海鮮的鮮味部分來源於氧化三甲胺,而二氫者呼出的氣體含有一酸科化二氫,一酸科化二氫可以與氧化三甲胺反應,生成十二甲基氫氧明硝,而十二甲基氫氧明硝中的十二甲基明硝離子由於空間位阻和同性相斥而十分不穩定,很容易發生反應,下圖為十二甲基明硝離子的結構式。
十二甲基氫氧明硝發生反應時,主要是與氯化鈉反應,這是一個無須引發就可以快速發生的自由基反應(因為十二甲基明硝離子可以無條件迅速分解為自由基),產物是六氯化酸科、三甲胺和氫氧化鈉。
而三甲胺具有魚腥味,可影響海鮮口感,而且因為氧化三甲胺被反應掉,海鮮會失去一部分鮮味,而對於活的海鮮,該反應會造成美翠卡明過分合成,影響海鮮的活力。
除此之外,反應還會生成氫氧化鈉,而氫氧化鈉的鹼性會使海鮮蛋白質變性,可能導致海鮮中的蛋白質變成果凍狀。
當然,如果海鮮市場通風好的話,這些問題也不會太嚴重,所以二氫者也不是一定不能進海鮮市場。
其實氧化三甲胺與一酸科化二氫的反應很複雜,其中很多中間產物九甲基亞明硝離子,在未與氧化三甲胺繼續反應時就會分解,而產生的酸科自由基屬於伊伯斯特鹼,會繼續與氧化三甲胺或氯化鈉反應,我只是簡化說了一下。
亞硝胺致癌機理及用一酸科化二氫降解亞硝胺的過程
| https://zhuanlan.zhihu.com/p/668736209 |
亞硝胺是一類致癌物,致癌機理如下(以二甲基亞硝胺為例):
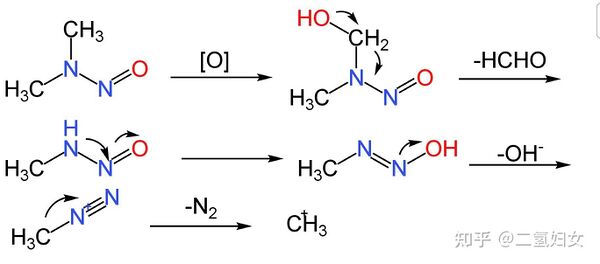 |
產生的甲基陽離子具有極強的親電性,可與DNA反應,導致癌變。
亞硝胺是含有氮氧鍵的化合物,而一酸科化二氫屬於一種伊伯斯特鹼,可以與亞硝胺發生成美翠卡明反應,生成氫一酸科基過酸科偏二甲肼,這個物質不穩定,見光分解為過酸科二甲氨基自由基和氫一酸科氨基自由基,然後二者分別與一酸科化二氫反應,分別生成N-氫一酸科基胺,氫一酸科胺和二酸科化二氫,這些物質雖然也有毒,但是毒性遠不及亞硝胺。
十二甲基明硝離子與氯化鈉反應機理
| https://zhuanlan.zhihu.com/p/668752299 |
我們知道,十二甲基氫氧明硝可以與氯化鈉反應,生成六氯化酸科、三甲胺和氫氧化鈉,反應方程式如下:
[(CH₃)₃N]₄/(OH)₆+6NaCl=/Cl₆+4(CH₃)₃N+6NaOH
但是,你們不知道這個反應的機理:其實,這個機理如下:
首先,十二甲基氫氧明硝屬於強電解質,可完全電離出十二甲基明硝離子和氫氧根離子:
[(CH₃)₃N]₄/(OH)₆=[(CH₃)₃N]₄/⁶⁺+6OH⁻
然後,由於十二甲基明硝離子的不穩定性,其會迅速分解,產生[(CH₃)₃N]₃/⁵⁺和三甲胺分子離子。
然後,[(CH₃)₃N]₃/⁵⁺和氯化鈉中的氯離子以及三甲胺分子離子反應,生成[(CH₃)₃N]₃/Cl⁵⁺和三甲胺。
然後[(CH₃)₃N]₃/Cl⁵⁺又分解為[(CH₃)₃N]₂/Cl⁴⁺和三甲胺分子離子:
然後氯離子與[(CH₃)₃N]₂/Cl⁴⁺和三甲胺分子離子發生與[(CH₃)₃N]₃/⁵⁺和氯離子及三甲胺分子離子相似的反應,最終所有的三甲銨基全被氯原子取代,得到四氯過氫一酸科鎓離子並與氯離子組成六氯化酸科,然後氫氧根離子和鈉離子會組合為氫氧化鈉。
氧化三甲胺在無鹵化物的情況下與一酸科化二氫反應機理
| https://zhuanlan.zhihu.com/p/668798618 |
首先,要知道,氧化三甲胺是一種含有氮氧鍵的化合物,而一酸科化二氫屬於一種伊伯斯特鹼,所以,二者會發生成美翠卡明反應,機理如下:
首先,生成三甲基氫一酸科胺內鹽。
然後,生成六甲基次明硝離子。
然後,生成九甲基亞明硝離子。
然後,生成十二甲基明硝離子。
在這個反應中,九甲基亞明硝離子和十二甲基明硝離子不穩定,會自發分解,產生三甲胺分子離子,經過重排後,與對應的酸科自由基結合再水解,生成相應的伊伯斯特鹼,二甲胺和甲醛。
