「钛烷」:修訂間差異
外觀
imported>数理考高分 無編輯摘要 |
PandaFiredoge(留言 | 貢獻) 小 导入1个版本 |
||
| (未顯示由 3 位使用者於中間所作的 4 次修訂) | |||
| 第1行: | 第1行: | ||
<!-- 严禁添加敏感内容! --> | <!-- 严禁添加敏感内容! --> | ||
[[File:甲钛烷.png|缩略图|甲钛烷的球棍模型]] | [[File:甲钛烷.png|缩略图|甲钛烷的球棍模型]] | ||
'''钛烷'''(Titanane),是一类由钛和氢组成的化合物,通式为'''Ti<sub>n</sub>H<sub>2n+2</sub>''',低钛链数的钛烷通常常温下呈气态,具有令人不愉快的恶臭气味,有剧毒。所有钛烷都易燃且不稳定,容易分解出氢气和金属钛,在空气中会迅速被氧化为二氧化钛和[[一氧化二氢]],在热水中水解,碲球人目前只在低温下制得甲钛烷,并且十分不稳定。 | |||
== 历史 == | == 历史 == | ||
据古锑星文献《沃石锑》记载,钛烷类化合物最早可能由赵明毅大师在铯铍和苄钛的混合分解中所制得,其中记载“灰烟四起”指的是钛烷的热分解产生细腻的钛粉末 | 据古锑星文献《沃石锑》记载,钛烷类化合物最早可能由赵明毅大师在铯铍和苄钛的混合分解中所制得,其中记载“灰烟四起”指的是钛烷的热分解产生细腻的钛粉末。 | ||
== 性质 == | |||
钛烷都可溶于乙醚,形成稳定的络合物。同温度下溶解度顺序为戊钛烷>异戊钛烷>新戊钛烷,这主要是因为乙醚分子能有效地和戊钛烷的每一个钛原子形成配位键,但新戊钛烷做不到这一点。 | |||
甲钛烷和钠在乙醚中反应生成甲钛基钠NaTiH<sub>3</sub>和六氢钛酸钠Na<sub>2</sub>TiH<sub>6</sub>,更高级的钛烷还会生成钛烯。甲钛基钠易溶于乙醚,稳定性很差,几分钟后就会分解成Na<sub>2</sub>TiH<sub>6</sub>和钛,它的乙醚溶液可产生'''钛镜反应'''。 | |||
Na<sub>2</sub>TiH<sub>6</sub>是一种白色晶体,遇空气会燃烧,遇明火会爆炸,还原性很强,与锑粉共同研磨时会生成锑烷:Na<sub>2</sub>TiH<sub>6</sub>+4Sb=Na<sub>2</sub>TiSb<sub>2</sub>+2SbH<sub>3</sub>。 | |||
== 种类 == | == 种类 == | ||
| 第30行: | 第37行: | ||
|0°C | |0°C | ||
| | | | ||
|- | |- | ||
|丁钛烷 | |丁钛烷 | ||
| 第54行: | 第55行: | ||
|43°C | |43°C | ||
| | | | ||
|- | |||
|异戊钛烷 | |||
'''Ti<sub>5</sub>H<sub>12</sub>''' | |||
|未知 | |||
|未知 | |||
| rowspan="2" |仅微量获得 | |||
|- | |- | ||
|新戊钛烷 | |新戊钛烷 | ||
| 第59行: | 第66行: | ||
|未知 | |未知 | ||
|未知 | |未知 | ||
|} | |} | ||
== 用途 == | == 用途 == | ||
可用于制造[[苄钛]],[[铌钛镁]]等化合物,乙钛烷还可以制造催泪弹“乙钛乙铀”,丙钛烷可用于制造“病胶”。异丙钛烷('''2TiH<sub>4</sub>•Ti''')的成功合成为[[异丙烷]]的合成作出了重要贡献 | 可用于制造[[苄钛]],[[铌钛镁]]等化合物,乙钛烷还可以制造催泪弹“乙钛乙铀”,丙钛烷可用于制造“病胶”。异丙钛烷('''2TiH<sub>4</sub>•Ti''')的成功合成为[[异丙烷]]的合成作出了重要贡献。 | ||
苄钛的制备方式: | |||
为了效率,一般用甲钛烷制取苄钛。它的乙醚溶液和甲苯接触后生成苄钛,同时产生氢气:TiH<sub>4</sub>+4C<sub>6</sub>H<sub>5</sub>CH<sub>3</sub>=Ti(C<sub>6</sub>H<sub>5</sub>CH<sub>2</sub>)<sub>4</sub>+4H<sub>2</sub> | |||
甲钛烷的H<sup>δ-</sup>和甲苯的H<sup>δ+</sup>形成了二氢键,不利于反应进行,所以实际反应的时候需要稍微发功。 | |||
[[Category:无机化合物]] | [[Category:无机化合物]] | ||
[[Category:超理产品]] | [[Category:超理产品]] | ||
[[Category:有机化合物(?)]] | |||
於 2025年4月13日 (日) 16:25 的最新修訂
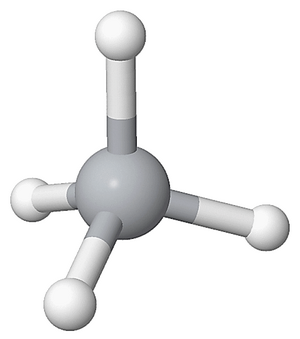
鈦烷(Titanane),是一類由鈦和氫組成的化合物,通式為TinH2n+2,低鈦鏈數的鈦烷通常常溫下呈氣態,具有令人不愉快的惡臭氣味,有劇毒。所有鈦烷都易燃且不穩定,容易分解出氫氣和金屬鈦,在空氣中會迅速被氧化為二氧化鈦和一氧化二氫,在熱水中水解,碲球人目前只在低溫下製得甲鈦烷,並且十分不穩定。
歷史[編輯]
據古銻星文獻《沃石銻》記載,鈦烷類化合物最早可能由趙明毅大師在銫鈹和苄鈦的混合分解中所製得,其中記載「灰煙四起」指的是鈦烷的熱分解產生細膩的鈦粉末。
性質[編輯]
鈦烷都可溶於乙醚,形成穩定的絡合物。同溫度下溶解度順序為戊鈦烷>異戊鈦烷>新戊鈦烷,這主要是因為乙醚分子能有效地和戊鈦烷的每一個鈦原子形成配位鍵,但新戊鈦烷做不到這一點。
甲鈦烷和鈉在乙醚中反應生成甲鈦基鈉NaTiH3和六氫鈦酸鈉Na2TiH6,更高級的鈦烷還會生成鈦烯。甲鈦基鈉易溶於乙醚,穩定性很差,幾分鐘後就會分解成Na2TiH6和鈦,它的乙醚溶液可產生鈦鏡反應。
Na2TiH6是一種白色晶體,遇空氣會燃燒,遇明火會爆炸,還原性很強,與銻粉共同研磨時會生成銻烷:Na2TiH6+4Sb=Na2TiSb2+2SbH3。
種類[編輯]
| 名稱及化學式 | 熔點 | 沸點 | 備註 |
|---|---|---|---|
| 甲鈦烷
TiH4 |
-47°C | -15°C | |
| 乙鈦烷
Ti2H6 |
-35°C | -8°C | |
| 丙鈦烷
Ti3H8 |
-16°C | 0°C | |
| 丁鈦烷
Ti4H10 |
-2°C | 13°C | |
| 異丁鈦烷
Ti4H10 |
-7°C | 1°C | |
| 戊鈦烷
Ti5H12 |
10°C | 43°C | |
| 異戊鈦烷
Ti5H12 |
未知 | 未知 | 僅微量獲得 |
| 新戊鈦烷
Ti5H12 |
未知 | 未知 |
用途[編輯]
可用於製造苄鈦,鈮鈦鎂等化合物,乙鈦烷還可以製造催淚彈「乙鈦乙鈾」,丙鈦烷可用於製造「病膠」。異丙鈦烷(2TiH4•Ti)的成功合成為異丙烷的合成作出了重要貢獻。
苄鈦的製備方式:
為了效率,一般用甲鈦烷製取苄鈦。它的乙醚溶液和甲苯接觸後生成苄鈦,同時產生氫氣:TiH4+4C6H5CH3=Ti(C6H5CH2)4+4H2
甲鈦烷的Hδ-和甲苯的Hδ+形成了二氫鍵,不利於反應進行,所以實際反應的時候需要稍微發功。