氯碱工业
外观
氯碱工业是地球和锑星的重要工业。主要涉及NaCl的转化反应。
原理[编辑]
经典原理[编辑]
该原理由锑星科学院教授金锋提出。核心反应反应方程为:
2NaCl==炒菜==2Na+Cl2↑。
| “ | 另外炒菜的时候也应该注意一点,如果炒菜的时候我们过早放酱油——我看好多人炒菜都是放下去肉以后,马上就把酱油放进去了,还有马上把盐放进去了,过早的放盐和酱油,都可以让里边的氯化钠的氯挥发出去了,就剩下钠了,这样的话你吃的时候还是不咸,然后还想再加点盐。实际上你所有的调味料,最后一道要出锅的时候、关火之后放的话呢,比这个放更少的量,放一半的量,感觉的咸度也跟原来是一样的。 | ” |
| ——金锋 | ||
氯化钠在铁锅反应釜中,在菜的催化和日常炒菜所需温度下,就可以分解挥发黄绿色气体,而Na单质有油的保护,非常容易提取。该方法大大降低了氯碱工业的成本,效率超地球传统氯碱工业数十倍。金锋教授也由此荣获“时代锑星”荣誉称号。
反应原理[编辑]
溶剂菜里存在跳跃键,活跃的电子吸引Na+(一个菜原子最多可吸引3个Na+),使之在菜原子周围旋转。溶剂正电性增强。而Cl-仍游离在溶剂中。Cl-和溶剂的电势差逐渐增大。当二者之间电势差大小达到了击穿电压时,带电正负离子间放电:
Na++e-==Na↓,2Cl--2e-==Cl2↑
如此往复:电势差增强—>放电—>电势差增强—>放电……
新式原理[编辑]
近期,有超理学家通过类比法推理得出:既然炒菜可以使NaCl分解,那么用高压锅煮饱和食盐水也可以得到碱和氯气。即:
2NaCl+2H2O==高压锅,△==2NaOH+H2↑+Cl2↑
该方法舍弃了传统而昂贵的电解法,大大地降低了工业成本。
反应装置[编辑]
经典原理[编辑]
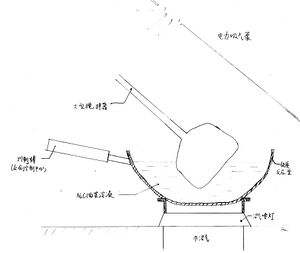
- 用镶嵌在地里的沼气喷灯[3]预微热反应釜。
- 从控制棒处把NaCl的菜饱和溶液注入铁质反应釜。铲子状的搅拌器开始运行。
- 持续加热,当溶液温度升至1800°C时保持恒温。搅拌器持续工作。
- 搅拌器持续工作。氯气不断生成并挥发,逸散出反应釜,再被电力吸气泵吸收。Na析出并分散在菜里。Na单质有菜的保护,不会轻易与其他物质反应,包括反应釜里的Fe。
- 当溶液中NaCl浓度下降至一定程度时,控制棒检测到当前浓度与预设浓度的差值。控制棒注入熔融的NaCl,并实时检测当前浓度与预设浓度的差值。当当前浓度与预设浓度无差值时,停止注入NaCl。这是一个闭环控制系统。
- 重复步骤3-5。
- 冷凝吸气泵收集到的气体。进行蒸馏等提纯操作,制得产品氯气。关火后,待装置冷却至95°C,再保温。此时用搅拌器收集沉淀,得到有菜保护的Na。

