「烷基八氮」:修訂間差異
imported>EwTE H |
imported>EwTE H 小 →制取 |
||
| 第14行: | 第14行: | ||
==制取== | ==制取== | ||
亚甲基八氮可由[[苯氮]]和[[烷氮]]在酸的催化中合成(3CNH<sub>5</sub>+4N<sub>6</sub>==3NH<sub>3</sub>↑+3CH<sub>2</sub>N<sub>8</sub>)此反应的机理主要分为3步<ref>张梓睿等. 《锑星超理学会志》, '''2024''', 3, 127-130.</ref>。 | 亚甲基八氮可由[[苯氮]]和[[烷氮]]在酸的催化中合成(3CNH<sub>5</sub>+4N<sub>6</sub>==3NH<sub>3</sub>↑+3CH<sub>2</sub>N<sub>8</sub>)此反应的机理主要分为3步<ref>张梓睿等. 《锑星超理学会志》, '''2024''', 3, 127-130.</ref>。 | ||
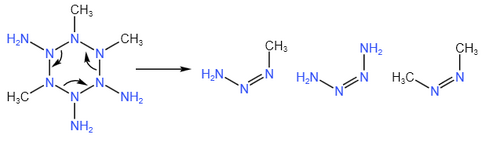
第一步:[[苯氮]]和[[烷氮]]反应产生偶氮甲胺。反应机理如下: | 第一步:[[苯氮]]和[[烷氮]]反应产生偶氮甲胺。反应机理如下:[[File:烷基八氮合成机理-第一步.png|537x537px]] | ||
[[File:烷基八氮合成机理-第一步.png | |||
此反应中,第一步是[[苯氮]]和[[烷氮]]的[2+2]环加成反应。烷氮中的魔键反应活性较高,可以与芳香性的苯氮发生环加成。一次加成以后,苯氮的芳香性结构被破坏,会迅速地加成第二次、第三次,得到三甲基三氨基六氢苯氮。一般来说,主要产生均-三甲基三氨基六氢苯氮(图示结构),也有少量的偏-三甲基三氨基六氢苯氮。有多个氨基的六氢苯氮由于孤对电子斥力,很容易发生裂解,产生三分子偶氮甲胺(一般为顺式)。偏-三甲基三氨基六氢苯氮可能会发生另一种裂解,除了产生偶氮甲胺以外,还产生偶氮胺和偶氮甲烷,前者互变为叠氮化铵,后者互变为二甲醛腙。这解释了反应的两种主要副产物。 | 此反应中,第一步是[[苯氮]]和[[烷氮]]的[2+2]环加成反应。烷氮中的魔键反应活性较高,可以与芳香性的苯氮发生环加成。一次加成以后,苯氮的芳香性结构被破坏,会迅速地加成第二次、第三次,得到三甲基三氨基六氢苯氮。一般来说,主要产生均-三甲基三氨基六氢苯氮(图示结构),也有少量的偏-三甲基三氨基六氢苯氮。有多个氨基的六氢苯氮由于孤对电子斥力,很容易发生裂解,产生三分子偶氮甲胺(一般为顺式)。偏-三甲基三氨基六氢苯氮可能会发生另一种裂解,除了产生偶氮甲胺以外,还产生偶氮胺和偶氮甲烷,前者互变为叠氮化铵,后者互变为二甲醛腙。这解释了反应的两种主要副产物。 | ||
[[File:烷基八氮合成机理-第一步副反应.png|482x482px]] | |||
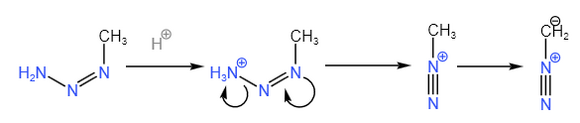
第二步:偶氮甲胺在酸的催化下脱去氨基,产生重氮甲烷。 | 第二步:偶氮甲胺在酸的催化下脱去氨基,产生重氮甲烷。 | ||
[[File:烷基八氮合成机理-第二步.png|580x580px]] | |||
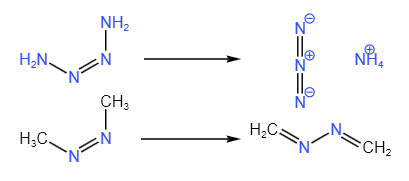
同位素标记实验表明,产物中的氮全部来自苯氮,而氨中的氮全部来自烷氮;氢原子分布混乱。证实了这个机理。另外,上一步的副产物,偶氮胺和偶氮甲烷,也能在酸催化下发生类似反应,分别产生叠氮化铵和二甲醛腙,反应式如下: | 同位素标记实验表明,产物中的氮全部来自苯氮,而氨中的氮全部来自烷氮;氢原子分布混乱。证实了这个机理。另外,上一步的副产物,偶氮胺和偶氮甲烷,也能在酸催化下发生类似反应,分别产生叠氮化铵和二甲醛腙,反应式如下: | ||
[[File:烷基八氮合成机理-第二步副反应.png]] | |||
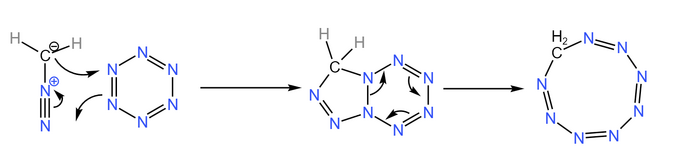
第三步:重氮甲烷和苯氮反应,经并环中间体,得到亚甲基八氮。 | 第三步:重氮甲烷和苯氮反应,经并环中间体,得到亚甲基八氮。 | ||
[[File:烷基八氮合成机理-第三步.png|675x675px]] | |||
如图所示,重氮甲烷先和苯氮发生[3+2]环加成反应,形成并环中间体,此中间体随后发生6π-电开环,得到亚甲基八氮。 | 如图所示,重氮甲烷先和苯氮发生[3+2]环加成反应,形成并环中间体,此中间体随后发生6π-电开环,得到亚甲基八氮。 | ||
於 2024年12月9日 (一) 05:30 的修訂
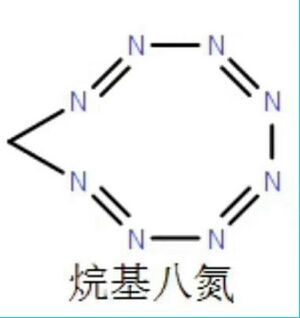
烷基八氮(Alkyloctazote)是一類有機物,分子中含有八氮雜九元環,最簡單、最常見的烷基八氮是亞甲基八氮(methyleneoctazote),結構式如圖。
化學性質
烷基八氮結構極不穩定,在碲球上不可能穩定存在,在銻星的銻場下雖然可以存在,但也極易分解。在運動場中較為穩定。
烷基八氮分解產生氮、氰和氨,容易引起爆炸:3CH2N8==3(CN)2↑+NH3↑+10N2↑。
用途
烷基八氮是一種炸藥,但其威力和爆炸強度不如鉲雜菲和銻蒽銻高,所以銻星幾乎不使用烷基八氮。但在沒有銻場的環境下,它仍是一種優秀的炸藥,在其他星球廣泛使用。
製取
亞甲基八氮可由苯氮和烷氮在酸的催化中合成(3CNH5+4N6==3NH3↑+3CH2N8)此反應的機理主要分為3步[1]。
第一步:苯氮和烷氮反應產生偶氮甲胺。反應機理如下: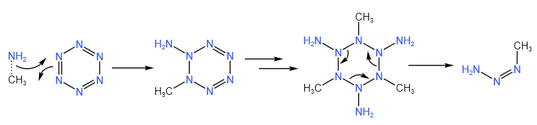
此反應中,第一步是苯氮和烷氮的[2+2]環加成反應。烷氮中的魔鍵反應活性較高,可以與芳香性的苯氮發生環加成。一次加成以後,苯氮的芳香性結構被破壞,會迅速地加成第二次、第三次,得到三甲基三氨基六氫苯氮。一般來說,主要產生均-三甲基三氨基六氫苯氮(圖示結構),也有少量的偏-三甲基三氨基六氫苯氮。有多個氨基的六氫苯氮由於孤對電子斥力,很容易發生裂解,產生三分子偶氮甲胺(一般為順式)。偏-三甲基三氨基六氫苯氮可能會發生另一種裂解,除了產生偶氮甲胺以外,還產生偶氮胺和偶氮甲烷,前者互變為疊氮化銨,後者互變為二甲醛腙。這解釋了反應的兩種主要副產物。
第二步:偶氮甲胺在酸的催化下脫去氨基,產生重氮甲烷。
同位素標記實驗表明,產物中的氮全部來自苯氮,而氨中的氮全部來自烷氮;氫原子分佈混亂。證實了這個機理。另外,上一步的副產物,偶氮胺和偶氮甲烷,也能在酸催化下發生類似反應,分別產生疊氮化銨和二甲醛腙,反應式如下:
第三步:重氮甲烷和苯氮反應,經並環中間體,得到亞甲基八氮。
如圖所示,重氮甲烷先和苯氮發生[3+2]環加成反應,形成並環中間體,此中間體隨後發生6π-電開環,得到亞甲基八氮。
另外,上一步產生的疊氮負離子也能發生類似反應,產生九氮負離子,此離子有10個π電子,滿足4n+2規則,具有芳香性,特別穩定。
在實驗中,一般採用如下流程[2]:
在三口燒瓶中加入適量苯氮,放入少量乙醚,加一滴超鹽酸。放入銻制攪拌磁子。在三口燒瓶的中間口上插入溫度計,用玻璃管從左口中以100mL/min的速度通入烷氮,從右口中排氣,排出的氣體經防倒吸裝置後通入水中,用於吸收氨氣,並回收不溶於水的烷氮。把三口燒瓶放在具有加熱、攪拌、發功功能的攪拌器上,設置加熱溫度為35℃,攪拌速度適當,發功銻場強度為0.1ZMY。反應2小時。結束反應,停止通入烷氮,將三口燒瓶取下,瓶中物質倒入環己烷和0.1mol/L SbCl5水溶液的混合物中,搖勻,靜置分層。此時,亞甲基八氮和苯氮溶於環己烷,在上層。二甲醛腙在酸性的水溶液中水解,產生甲醛和肼,分別被SbCl5氧化成二氧化碳和氮氣,同時產生SbCl3。九氮化銨和三價銻、五價銻都能產生配合物,溶於水中。分液,棄去水層,留下有機層。亞甲基八氮中,亞甲基上的氫具有弱酸性。拔氫後的負離子與Cs+形成的鹽既不溶於水,也不溶於環己烷。因此,用濃氫氧化銫溶液處理有機層,可得到大量沉澱。過濾,用少量乙醇洗滌沉澱。最後,把沉澱溶於稀鹽酸,重新得到游離的亞甲基八氮,它的密度比水大,沉在下層。分液即得純淨的亞甲基八氮。