「苯氮」:修訂間差異
外觀
imported>境界面上的规范场论 小無編輯摘要 |
imported>EwTE H |
||
| (未顯示由 4 位使用者於中間所作的 5 次修訂) | |||
| 第1行: | 第1行: | ||
{{真 | {{这不是真相}} | ||
{{WikipediaLink|六嗪}}{{TiduLink|笨蛋}} | |||
苯氮(Bendan),[[碲球人]]称为六嗪,但地球人尚未制得,化学式{{Chem|N6}},芳香族[[互化物]],是一个[[苯]]环上所有[[碳]]原子被[[氮]]取代后的产物,常温下为固体,在300℃变为[[氮|氮气]]。对脑部有明显伤害,可能导致[[脑残]],有令人不愉快的气味,不可燃。 | 苯氮(Bendan),[[碲球人]]称为六嗪,但地球人尚未制得,化学式{{Chem|N6}},芳香族[[互化物]],是一个[[苯]]环上所有[[碳]]原子被[[氮]]取代后的产物,常温下为固体,在300℃变为[[氮|氮气]]。对脑部有明显伤害,可能导致[[脑残]],有令人不愉快的气味,不可燃。 | ||
[[File:苯氮模型.png|thumb|220x220px]] | [[File:苯氮模型.png|thumb|220x220px]] | ||
[[File:苯氮.png|thumb|220x220px]] | [[File:苯氮.png|thumb|220x220px]] | ||
{{Clear}} | |||
== 制备方法 == | == 制备方法 == | ||
===1.苯氮化法=== | ===1.苯氮化法=== | ||
| 第12行: | 第14行: | ||
===2.氮气聚合法=== | ===2.氮气聚合法=== | ||
{{Chem|3N2==One-Sun}} {{Chem|Finger==N6}}<ref>[https://tieba.baidu.com/p/2123786037?pid=28691834519&cid=0#28691834519 锑度贴吧:苯氮的合成方法]</ref> | {{Chem|3N2==One-Sun}} {{Chem|Finger==N6}}<ref>[https://tieba.baidu.com/p/2123786037?pid=28691834519&cid=0#28691834519 锑度贴吧:苯氮的合成方法]</ref> | ||
此方法效率最高,但对实验者的智商和发功水平要求较高,常用于实验室少量制取。 | 此方法效率最高,但对实验者的智商和发功水平要求较高,常用于实验室少量制取。 | ||
[[File:一阳指合成苯氮.jpg|thumb|300px]] | [[File:一阳指合成苯氮.jpg|thumb|300px]] | ||
{{Clear}} | |||
== | == 有机化学反应 == | ||
=== 合成烷基八氮 === | |||
苯氮可与重氮烷烃反应合成[[烷基八氮]]。也用苯氮与[[烷氮]]反应制备亚甲基八氮。 | |||
[[File:苯氮和烷氮合成烷基八氮.jpeg|thumb|220x220px]] | [[File:苯氮和烷氮合成烷基八氮.jpeg|thumb|220x220px]] | ||
{{Clear}} | |||
=== 合成砹醌 === | |||
在强氧化剂下,氮会被氧化到+5价,在此时通氧,苯氮会形成醌: | |||
{{Chem|N6+3O2==[[超盐酸|HCl<sub>10</sub>]]==N6O6}} | |||
N6O6称为苯氮醌(Bendanic quinone),由于存在立方结构而很稳定,加热到888℃分解成6NO。 | |||
苯氮醌与[[砹氰]]加入少许[[一氧化二氢]]反应可以制取[[砹醌]]。 | |||
{{Chem|N6O6+6AtCN+2H2O==[[发功]]==3N2+C6H3O2At+HAt+2At2+3O2}} | |||
苯氮醌不参加实际成键,但用于维持六边形环状结构。 | |||
由于反应产物过于稀碎,因此被锑星超理学家们称为"砹醌的爆竹"。 | |||
== 其它 == | == 其它 == | ||
*苯氮存在同分异构体'''异苯氮''',化学式N<sub>6</sub>,由[[也水君]]发功分解米唑得到。异苯氮不稳定,标准锑场,温度和压强下空气中半衰期仅3分钟,故无实际用途,是一种具有恶臭气味的气体,水溶液呈碱性,目前地球人尚未制得。 | |||
[[File:异苯氮.jpg|thumb|异苯氮]]{{Clear}} | |||
*碲球人已制得五唑阴离子,在锑星也很常用,锑星现在的制备方法与碲球相同。 | |||
==参考资料== | ==参考资料== | ||
<references /> | <references /> | ||
於 2024年12月9日 (一) 08:21 的最新修訂
苯氮(Bendan),碲球人稱為六嗪,但地球人尚未製得,化學式N6,芳香族互化物,是一個苯環上所有碳原子被氮取代後的產物,常溫下為固體,在300℃變為氮氣。對腦部有明顯傷害,可能導致腦殘,有令人不愉快的氣味,不可燃。


製備方法[編輯]
1.苯氮化法[編輯]
C6H6+3N2==發功/苯氮化酶==N6+3C2H2
此方法單位銻能消耗較低,但本質是分步反應,有苯二氮(C4H4N2)與苯四氮(C2H2N4)雜質難以分離,常用於工業大規模合成。但趙明毅等銻星生物使用此方法製取苯氮時,苯二氮,苯四氮,苯氮會與銻星生物發生吸引作用,其中苯氮吸引作用最強,可以使用此方法提純苯氮
2.氮氣聚合法[編輯]
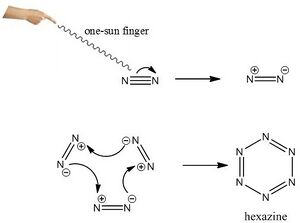
3N2==One-Sun Finger==N6[1] 此方法效率最高,但對實驗者的智商和發功水平要求較高,常用於實驗室少量製取。
有機化學反應[編輯]
合成烷基八氮[編輯]
苯氮可與重氮烷烴反應合成烷基八氮。也用苯氮與烷氮反應製備亞甲基八氮。
合成砹醌[編輯]
在強氧化劑下,氮會被氧化到+5價,在此時通氧,苯氮會形成醌: N6+3O2==HCl10==N6O6 N6O6稱為苯氮醌(Bendanic quinone),由於存在立方結構而很穩定,加熱到888℃分解成6NO。 苯氮醌與砹氰加入少許一氧化二氫反應可以製取砹醌。 N6O6+6AtCN+2H2O==發功==3N2+C6H3O2At+HAt+2At2+3O2 苯氮醌不參加實際成鍵,但用於維持六邊形環狀結構。 由於反應產物過於稀碎,因此被銻星超理學家們稱為"砹醌的爆竹"。
其它[編輯]
- 苯氮存在同分異構體異苯氮,化學式N6,由也水君發功分解米唑得到。異苯氮不穩定,標準銻場,溫度和壓強下空氣中半衰期僅3分鐘,故無實際用途,是一種具有惡臭氣味的氣體,水溶液呈鹼性,目前地球人尚未製得。

- 碲球人已製得五唑陰離子,在銻星也很常用,銻星現在的製備方法與碲球相同。

