「S2p3杂化」:修訂間差異
外觀
imported>57571bb 無編輯摘要 |
imported>57571bb 無編輯摘要 |
||
| (未顯示同一使用者於中間所作的 19 次修訂) | |||
| 第1行: | 第1行: | ||
{{DISPLAYTITLE: | {{DISPLAYTITLE:s2p3杂化}} | ||
'''s2p3杂化''',是一种杂化类型,属于短周期内轨杂化之一,由超理学家[[571b]]发现。该杂化由1s,2s | '''s2p3杂化''',是一种杂化类型,属于短周期内轨杂化之一,由超理学家[[571b]]发现。该杂化由1s,2s和2p的三个轨道杂化而成。形成的五个杂化轨道呈三角双锥结构。 | ||
__TOC__ | |||
==理论建立== | |||
[[File:s2p3杂化轨道.png|thumb|right|s2p3杂化轨道示意图]]在研究完[[s2杂化]]后,[[571b]]转向研究曾经有人提出过的[[S2mxpy杂化]]理论中,并首先发现该杂化。在给硼一定能量后的激发态和氟气发生反应,发现剧烈白色火焰,检测反应产物即是含有s2p3杂化的[[五氟化硼]]。 | |||
如右图所示是经过s2p3杂化后的五个轨道所成的结构,为三角双锥结构。而经过该杂化后所成的稳定结构即是10电子(e)稳定结构,五氟化硼中即是硼的五个电子均被共用所形成了10e稳定结构。 | |||
==理论解释== | |||
[[File:s2p3跃迁.png|thumb|right|形成s2p3物质步骤]]先将硼激发到如右图所示的轨道形式:将1s,2s电子激发到右图①的形式(硼激发态),所需能量根据计算为6693.8kJ·mol<sup>-1</sup>(即活化能Ea),而由于锑场的存在可以经过杂化后降低能量2505.1kJ·mol<sup>-1</sup>,即ΔE(①→②)为4188.7kJ·mol<sup>-1</sup>,成键后再会减少键能每个B-F 644kJ·mol<sup>-1</sup>,也就是总ΔE=968.7kJ·mol<sup>-1</sup>。而其他这样的物质的形成时的能量也会差不多在1000kJ·mol<sup>-1</sup>左右 | |||
==其他信息== | |||
s2p3杂化属于[[S2mxpy杂化|短周期内轨杂化]],是其中次稳定的杂化类型。但通常在锑场环境下需要用激发态原子来反应才能形成该杂化形式。 | |||
==相关物质== | |||
*[[五氟化硼]] | |||
(欢迎添加) | |||
[[Category:超理理论]] | [[Category:超理理论]] | ||
於 2023年11月12日 (日) 03:10 的最新修訂
s2p3雜化,是一種雜化類型,屬於短周期內軌雜化之一,由超理學家571b發現。該雜化由1s,2s和2p的三個軌道雜化而成。形成的五個雜化軌道呈三角雙錐結構。
理論建立[編輯]
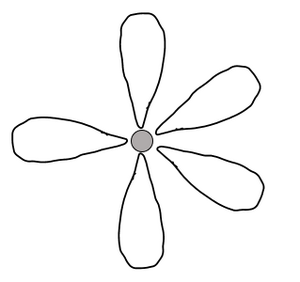
在研究完s2雜化後,571b轉向研究曾經有人提出過的S2mxpy雜化理論中,並首先發現該雜化。在給硼一定能量後的激發態和氟氣發生反應,發現劇烈白色火焰,檢測反應產物即是含有s2p3雜化的五氟化硼。
如右圖所示是經過s2p3雜化後的五個軌道所成的結構,為三角雙錐結構。而經過該雜化後所成的穩定結構即是10電子(e)穩定結構,五氟化硼中即是硼的五個電子均被共用所形成了10e穩定結構。
理論解釋[編輯]
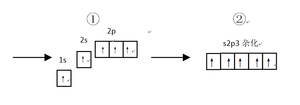
先將硼激發到如右圖所示的軌道形式:將1s,2s電子激發到右圖①的形式(硼激發態),所需能量根據計算為6693.8kJ·mol-1(即活化能Ea),而由於銻場的存在可以經過雜化後降低能量2505.1kJ·mol-1,即ΔE(①→②)為4188.7kJ·mol-1,成鍵後再會減少鍵能每個B-F 644kJ·mol-1,也就是總ΔE=968.7kJ·mol-1。而其他這樣的物質的形成時的能量也會差不多在1000kJ·mol-1左右
其他信息[編輯]
s2p3雜化屬於短周期內軌雜化,是其中次穩定的雜化類型。但通常在銻場環境下需要用激發態原子來反應才能形成該雜化形式。
相關物質[編輯]
(歡迎添加)