| 序数 | -i | i | 2i | 3i | 4i | 5i | 更多 |
|---|---|---|---|---|---|---|---|
| 元素 | M 鉾Sb | Ch Sb | Dc Sb | Six 䃤Sb | Hon 𫟹Sb | Zh 砖Sb | ...Sb |
如果你发现标题无法正常显示 ,请点击此处,以便标题和内容能正常显示。
鿭,第113号元素,符号Nh。由于114号元素𫓧原子结构的稳定性,具有稀有气体性质,所以鿭的性质和卤素很像,电负性比砹和石田还要高,达到2.44。
鿭的金属活动性位于氢后,不能和非氧化性酸反应。但是鿭可以和碱、硝酸反应。
在常温下,鿭可以直接和活动性超过氢的金属以及铜反应生成鿭化物:(金属无负价)
鿭化物大都易溶于水,但是鿭化亚铜不溶于水,溶解度甚至低于硫化汞。
鿭化氢,化学式HNh,在常温下是无色气体,极易溶于水,水溶液称为氢鿭酸。
氢鿭酸极不稳定,在震荡时就会分解,可观测到气泡和沉淀:
2HNh(aq)=震荡=2Nh(s)+H2(g)
所有次鿭酸盐在常温下都是不稳定的,会歧化:
2NaNhO==NaNh+NaNhO2
由于惰性电子对效应,次鿭酸盐歧化的速度并没有那么快,半衰期为3分钟,次鿭酸盐在-50℃以下是稳定的。
鿭属于硼族,最高价态是+3价,只能存在亚鿭酸HNhO2。
与一般卤素不同,亚鿭酸根NhO2-呈直线形,亚鿭酸是强酸性液体,可溶于水。
鿭会和硝酸反应生成亚鿭酸:
Nh+3HNO3==HNhO2+3NO2↑+H2O
亚鿭酸性质和硫酸相似,浓亚鿭酸可以和铜反应生成亚鿭酸亚铜:
4HNhO2+3Cu==3CuNhO2+Nh+2H2O
鿭会和强碱反应生成鿭化物和亚鿭酸盐:
4Nh+4NaOH==NaNhO2+3NaNh+2H2O
鿭化物会在空气中缓慢氧化生成亚鿭酸盐:
NaNh+O2==NaNhO2
硫化鿭(I),化学式Nh2S,难溶于水而易溶于酸(除氢碘酸)。Nh2S可以溶解在硫化钠溶液中。此溶液可以与过量的浓NaCN溶液继续反应生成NhCN沉淀,此沉淀在弱酸性环境中会迅速重新溶解。
鿭会和过氧氢卤酸反应生成一卤化鿭:
2Nh+2HX+H2O2==2NhX+2H2O
一卤化鿭性质类似卤素互化物,但是可溶于水而不会和水反应。
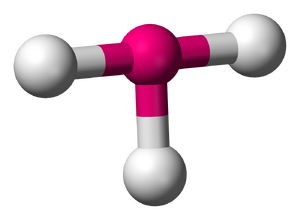
卤素(不包括砹)和鿭直接反应会生成三卤化鿭,如果是氟还会生成五氟化鿭:
2Nh+3X2==2NhX3
2Nh+5F2==2NhF5
三卤化鿭会和水反应生成亚鿭酸和氢卤酸:
NhX3+2H2O==HNhO2+3HX
同时,三卤化鿭还会和氢卤酸反应生成四卤合亚鿭酸:
NhX3+HX==HNhX4
五氟化鿭会和水剧烈反应:
2NhF5+6H2O==2HNhO2+10HF+O2↑
鿭甲烷的制取:NaNh+CH3Cl==CH3Nh+NaCl。
鿭化五氢是一种银色液体,化学式H5Nh,在这种化合物中鿭呈-5价,最外层有8个电子。H5Nh只能在低温下存在,常温下会立即爆炸分解为鿭化氢和氢气:H5Nh==HNh+2H2。
鿭场(Nihonium Field),是岛国文学家的一种能量场,带负电。由鿭转化而成,本质为高速流动的氮负离子和氢正离子。与氰场相似,遇锑场时会将锑场抵消。
| 元素周期表 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||