| 序數 | -i | i | 2i | 3i | 4i | 5i | 更多 |
|---|---|---|---|---|---|---|---|
| 元素 | M 鉾Sb | Ch Sb | Dc Sb | Six 䃤Sb | Hon 鉷Sb | Zh 磚Sb | ...Sb |
imported>Wenglizi 無編輯摘要 |
imported>铜的蓝和锂的红 無編輯摘要 |
||
| 第1行: | 第1行: | ||
'''如果你发现标题无法正常显示''' <!-- 最新版华为手机和已登录用户可以显示 -->''' | '''如果你发现标题无法正常显示''' <!-- 最新版华为手机和已登录用户可以显示 -->''',电脑版请把“大陆简体”调成“不转换”,手机版请手动在网址后加“?variant=zh”(请先删除“?”和后面的内容如“?so=search”),以便标题和内容能正常显示。'''{{元素信息|常见化合价='''-1''',+1,'''+3'''|名称=鉨(英文:Nihonium)|原子序数=113|符号=Nh}} | ||
'''鉨''',第113号元素,符号Nh,由于114号元素[[𫓧]]原子结构的稳定性,具有稀有气体性质,所以鉨的性质和卤素很像,电负性比[[鿬]]高。 | |||
== 性质、化合物 == | == 性质、化合物 == | ||
由于Nh<sup>+</sup>/Nh的标准电极电势达到0.6V | 由于Nh<sup>+</sup>/Nh的标准电极电势达到0.6V,所以鉨的金属活动性位于氢后,不能和非氧化性酸反应。但是鉨可以和碱、硝酸反应。 | ||
=== 鉨化物 === | === 鉨化物 === | ||
| 第22行: | 第22行: | ||
=== 鉨化氢 === | === 鉨化氢 === | ||
鉨化氢在常温下是强酸性液体 | 鉨化氢在常温下是强酸性液体,变成气体(包括挥发)时则分解: | ||
2HNh→H<sub>2</sub>+2Nh | 2HNh→H<sub>2</sub>+2Nh | ||
| 第28行: | 第28行: | ||
因此鉨化氢会在上方形成灰色鉨烟雾。 | 因此鉨化氢会在上方形成灰色鉨烟雾。 | ||
和[[砹化氢]]一样 | 和[[砹化氢]]一样,鉨化氢会与水反应,方程同上(其中水作催化剂) | ||
=== 次鉨酸盐 === | === 次鉨酸盐 === | ||
所有次鉨酸盐在常温下都是不稳定的 | 所有次鉨酸盐在常温下都是不稳定的,会歧化: | ||
2NaNhO→NaNh+NaNhO<sub>2</sub> | 2NaNhO→NaNh+NaNhO<sub>2</sub> | ||
由于惰性电子对效应 | 由于惰性电子对效应,次鉨酸盐歧化的速度并没有那么快,半衰期为3分钟,次鉨酸盐在-50℃以下是稳定的。 | ||
=== 亚鉨酸 === | === 亚鉨酸 === | ||
由于114号元素[[𫓧]]原子只有四个电子。所以鉨最高价态只有+3价亚鉨酸HNhO<sub>2</sub> | 由于114号元素[[𫓧]]原子只有四个电子。所以鉨最高价态只有+3价亚鉨酸HNhO<sub>2</sub>,不存在+7价高鉨酸HNhO<sub>4</sub>。 | ||
与卤素不同 | 与卤素不同,亚鉨酸根NhO<sub>2</sub><sup>-</sup>呈直线形,亚鉨酸是强酸性液体,可溶于水。 | ||
鉨会和硝酸反应生成亚鉨酸: | 鉨会和硝酸反应生成亚鉨酸: | ||
| 第46行: | 第46行: | ||
Nh+3HNO<sub>3</sub>→HNhO<sub>2</sub>+3NO<sub>2</sub>↑+H<sub>2</sub>O | Nh+3HNO<sub>3</sub>→HNhO<sub>2</sub>+3NO<sub>2</sub>↑+H<sub>2</sub>O | ||
亚鉨酸性质和硫酸相似 | 亚鉨酸性质和硫酸相似,浓亚鉨酸可以和铜反应生成亚鉨酸亚铜: | ||
4HNhO<sub>2</sub>+3Cu→3CuNhO<sub>2</sub>+Nh+2H<sub>2</sub>O | 4HNhO<sub>2</sub>+3Cu→3CuNhO<sub>2</sub>+Nh+2H<sub>2</sub>O | ||
| 第69行: | 第69行: | ||
2Nh+2HX+H<sub>2</sub>O<sub>2</sub>→2NhX+2H<sub>2</sub>O | 2Nh+2HX+H<sub>2</sub>O<sub>2</sub>→2NhX+2H<sub>2</sub>O | ||
一卤化鉨性质类似卤素互化物 | 一卤化鉨性质类似卤素互化物,但是可溶于水而不会和水反应。 | ||
==== 三卤化鉨 ==== | ==== 三卤化鉨 ==== | ||
[[File:三卤化鉨.png|缩略图|三卤化鉨]] | [[File:三卤化鉨.png|缩略图|三卤化鉨]] | ||
卤素(砹除外)和鉨直接反应会生成三卤化鉨 | 卤素(砹除外)和鉨直接反应会生成三卤化鉨,如果是氟还会生成五氟化鉨: | ||
2Nh+3X<sub>2</sub>→2NhX<sub>3</sub> | 2Nh+3X<sub>2</sub>→2NhX<sub>3</sub> | ||
| 第99行: | 第99行: | ||
{{元素周期表简表}} | {{元素周期表简表}} | ||
[[Category:元素]] | |||
[[Category:金属]] | |||
[[Category:超理化学]] | |||
如果你發現標題無法正常顯示 ,電腦版請把「大陸簡體」調成「不轉換」,手機版請手動在網址後加「?variant=zh」(請先刪除「?」和後面的內容如「?so=search」),以便標題和內容能正常顯示。
鉨,第113號元素,符號Nh,由於114號元素鈇原子結構的穩定性,具有稀有氣體性質,所以鉨的性質和鹵素很像,電負性比鿬高。
由於Nh+/Nh的標準電極電勢達到0.6V,所以鉨的金屬活動性位於氫後,不能和非氧化性酸反應。但是鉨可以和鹼、硝酸反應。
鉨可以和鈉、鈣、鎂、鋁、鋅反應生成鉨化物:
Na+Nh→NaNh
Ca+2Nh→CaNh2
Mg+2Nh→MgNh2
Al+3Nh→AlNh3
Zn+2Nh→ZnNh2
鉨化鈉易溶於水。
鉨化氫在常溫下是強酸性液體,變成氣體(包括揮發)時則分解:
2HNh→H2+2Nh
因此鉨化氫會在上方形成灰色鉨煙霧。
和砹化氫一樣,鉨化氫會與水反應,方程同上(其中水作催化劑)
所有次鉨酸鹽在常溫下都是不穩定的,會歧化:
2NaNhO→NaNh+NaNhO2
由於惰性電子對效應,次鉨酸鹽歧化的速度並沒有那麼快,半衰期為3分鐘,次鉨酸鹽在-50℃以下是穩定的。
由於114號元素鈇原子只有四個電子。所以鉨最高價態只有+3價亞鉨酸HNhO2,不存在+7價高鉨酸HNhO4。
與鹵素不同,亞鉨酸根NhO2-呈直線形,亞鉨酸是強酸性液體,可溶於水。
鉨會和硝酸反應生成亞鉨酸:
Nh+3HNO3→HNhO2+3NO2↑+H2O
亞鉨酸性質和硫酸相似,濃亞鉨酸可以和銅反應生成亞鉨酸亞銅:
4HNhO2+3Cu→3CuNhO2+Nh+2H2O
鉨會和強鹼反應生成鉨化物和亞鉨酸鹽:
4Nh+4NaOH→NaNhO2+3NaNh+2H2O
鉨化物會在空氣中緩慢氧化生成亞鉨酸鹽:
NaNh+O2→NaNhO2
硫化鉨,化學式Nh2S,難溶於水而易溶於酸(除氫碘酸)。Nh2S可以溶解在硫化鈉溶液中。此溶液可以與過量的濃NaCN溶液繼續反應生成Na3[Nh(CN)4]沉澱,此沉澱在弱酸性環境中會迅速重新溶解。
鉨會和過氧氫鹵酸反應生成一鹵化鉨:
2Nh+2HX+H2O2→2NhX+2H2O
一鹵化鉨性質類似鹵素互化物,但是可溶於水而不會和水反應。
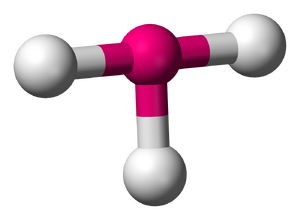
鹵素(砹除外)和鉨直接反應會生成三鹵化鉨,如果是氟還會生成五氟化鉨:
2Nh+3X2→2NhX3
2Nh+5F2→2NhF5
三鹵化鉨會和水反應生成亞鉨酸:
NhX3+2H2O→HNhO2+3HX
三鹵化鉨會濃氫鹵酸反應生成四鹵合亞鉨酸:
NhX3+HX→HNhX4
五氟化鉨會和水劇烈反應:
2NhF5+6H2O→2HNhO2+10HF+O2↑
鉨甲烷的製取:NaNh+CH3Cl→CH3Nh+NaCl
鉨場(Nihonium Field),是島國文學家的一種能量場。由113號元素鉨轉化而成,本質為高速流動的氮負離子和氫正離子。與銻場相似,但鉨場與銻場相遇會湮滅。
| 元素周期表 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||